近二十年来,生物工夫药物得以迅猛繁荣。遵循BCC Research的一份讲演,生物造剂的环球出售额正在2015年抵达2000亿美元,到2019岁晚估计将赶过3860亿美元。个中,抗体类药物霸占宏壮份额。过去30年中,共有63个抗体药物进入商场。抗体药物繁荣过程中有少少要紧里程碑式的事项,整体请见图1。
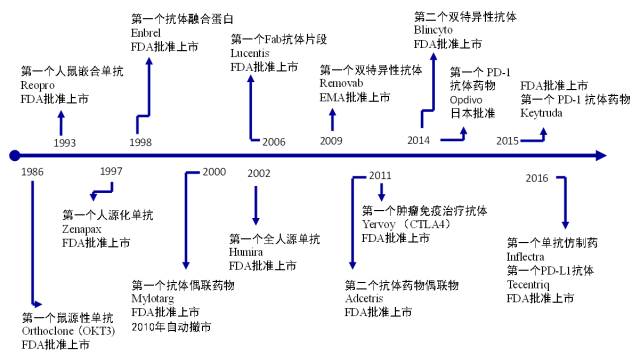
何如举办体例性药理学评议是抗体药物的一个要紧课题。药理学是磋议机体与药物互相效力的一门科学,药物对机体的效力合键展现为有用性以及平安性,而机体对药物的效力则归属于药代动力学的磋议范围,网罗吸取、散布、代谢及渗出等体内处分进程。药代动力学是批注药物有用性及平安性的物质本原,其要紧性无须置疑。因为药代动力学磋议药物标的自己为认识物,追踪其体内繁杂的动态进程,其难度与侦查药物对机体的效应是千差万此表。而生物认识工夫动作PK磋议的工夫撑持,拥有决策性旨趣。然而生物认识工夫频频会碰到良多“难合”或“瓶颈”性题目。分表是有别于幼分子药物,抗体类药物整体与内源性分子近似、表观分子不相仿、组织不确定性以及非预期的多向活性等特征,于是正在生物体内的药物处分机造有其分表性和繁杂性,极大的增进了磋议难度。正在药代动力学磋议进程中,还存正在其余一个题目即抗药性抗体(ADA)评议,ADA可以会对PK磋议结果出现明显性影响,何如对ADA举办体例性、科学性评议是目前的急迫性课题。分表是跟着抗体工程工夫的繁荣,抗体研发趋向曾经不控造于鼠源向人源化、全人抗体的繁荣,更趋于多效力化(双/多特异性抗体)、幼型化(以雷珠单抗为代表的抗体片断)和精准化(抗体药物偶联物(ADC))偏向的研发。抗体种别多样性的出现,不只需求多种认识措施及平台工夫的组合,更是对正确和强大的生物认识措施的开采和验证的需求日益拉长,并请求出现的数据经得起羁系审查。本文将扼要回忆抗体药物PK、ADA的评议的法例和认识应对战术两方面的转机进程,以及浅讲国内合系范围行业发显露状。
看待生物大分子药物认识措施,可认为公共所熟知的即是守旧的酶联免疫吸附措施(ELISA),但何如创造一个满意药物评议需求及切合法例请求的措施并不是任何一个实行室都能随便达成的,其需求多量表面及实验体会的几次“检验”。况且,因为ELISA措施受到通量低、聪颖度低、措施不乱性以及枢纽试剂(包被抗体和检测抗体)难以获取等工夫性壁垒,新工夫平台正正在连接的闪现如MSD、Gyros、Singulex、multiplex、Biacore等,另表LC-MS/MS反抗体定量认识的磋议也得回较大的繁荣,为多样化类型抗体类药物的PK评议供给有力保护(图2)。
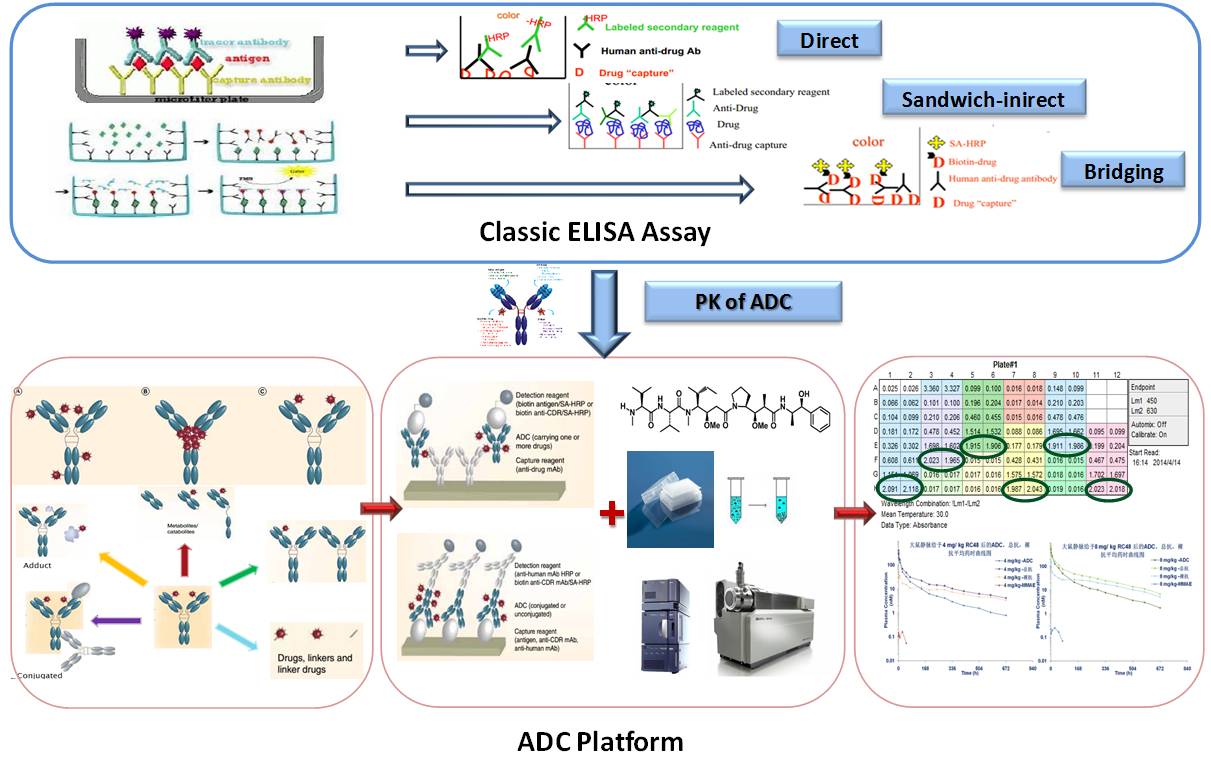
措施学验证是一共试验数据牢靠的根本保障,创造慎密客观的措施学验证的规范是药动学磋议的本原,是得回科学客观结果的根本保护。跟着生物认识工夫的连接更新以及正在生物认识范围体会的连接累积,人们也正在连接的搜检现有措施学样板性的科学性及实用性,从而胀动措施学行业规范履历了动态繁荣进程。
1990年之前哨法验证没有同一的行业规范,历时十年原委两次生物认识措施验证研讨会的召开,FDA于2001年发表初版措施学验证领导规定,并于2013年草拟了新的措施学验证草案;欧盟药物机构(EMA)从2008年始筹备对生物认识措施验证的样板,共履历了观点性文献、领导文献草案(2009年)、搜集看法和最终颁布等阶段于2012年发表生物认识措施学验证法例;该领导规定初度总共、明晰提出了生物大分子药物认识措施验证的目标和承受规范。即使我国药物研发滞后于西方兴隆国度,但近年来繁荣速率可谓惊人,分表是中国国度食物药品监视经管总局(CFDA)于2015年正在药典中对生物认识措施学验证的条款举办了体例的划定,这代表我国国度规范曾经渐渐与宇宙接轨,对胀动我国PK生物认识繁荣拥有要紧旨趣。
抗体药物研发进程中最大的体贴点之一是其是否可以诱导出现抗药性抗体(anti-drug antibody,ADA)。抗药性抗体能对药物透露、药物代谢动力学、药物效应动力学等变成影响,乃至激励重要平安性事项,加倍是对内源性因素药物而言,后果往往更为重要,如 EPO类药物出现的抗体能中和内源性EPO导致的PRCA,表源性IFN-β惹起的中和抗体与内源IFN β造成免疫复合物而激活补体,长效VII因子惹起的中和抗体导致加重原有出血方向等。所以抗体药物的免疫原性惹起了临床医师、药企及羁系机构的高度体贴。为了评估生物药物的免疫原性,以及将实行结果与合系事项相干起来,正在临床前磋议和临床磋议中,开采牢靠的可以有用评估抗药抗体的认识措施至合要紧。
因为抗药性抗体的出现拥有阶段性特征,分歧期间段的抗体亚型存正在差别性的;况且机体正在给药后药物以及内源性分子浓度程度的“扰乱”均会影响认识结果,故抗药性抗体认识措施应确凿、聪颖、特异、耐用,能检测出网罗IgG和IgM等全数亚型,同时基于危机采用多方针检测战术评议ADA,遵照筛选认识、确证认识、中和认识等举办逐层认识(图3)。目前推进行使的措施有直接或桥接酶联免疫吸附认识(ELISA)、放射免疫浸淀认识(RIPA)、轮廓等离子体共振(SPR)等,而目前免疫原性的磋议曾经拓展到了诸如MSD、Gyros、Singulex等更进步的认识平台,以满意越来越苛苛的评议规范的请求。
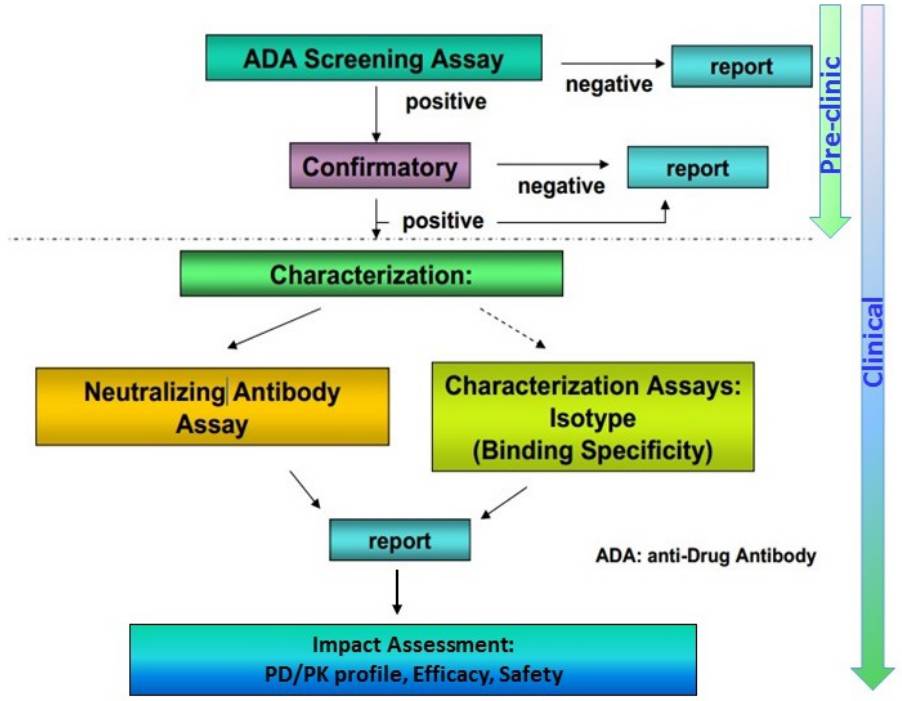
即使现阶段免疫原性认识措施磋议曾经得到了长足的进取,但正在实验中仍面对诸多要紧的或枢纽性题目,网罗:何如分身非临床及临床阶段磋议措施的需求;何如拔取及获取阳性比照(Positive Control,PC);是否需求或何如发展“不乱性”验证目标;何如低落药物或内源性分子对ADA磋议措施的影响;何如评议分歧认识平台磋议结果的“不相仿性”等。上述题目往往伴跟着免疫原性磋议的一共实验进程,需求正在以后的磋议中渐渐的办理并美满。
正在抗药性抗体认识措施样板性同意方面,EMA和FDA动作先行者曾经推出了一系列相应的指南。EMA于2006年头次创议草拟同意合于疗养性卵白免疫原性评议指南,并于2008年4月生效(EMEA/CHMP/BMWP/14327/2006),2015年,EMA对2008版指南又举办更新纠正,对认识战术个人举办更为详尽地描摹先容,针对分歧题目给出必然的办理计划和应对步伐。基于单克隆抗体的分表性,2012年,EMA特意针对单克隆抗体免疫原性认识同意出补充版指南。FDA于2009年头度推出疗养性卵白免疫原性磋议措施学开采指南草案,并于2016年又出台了新版本的免疫原性评估草案,FDA对旧版本的个人实质举办了修订。而我国目前尚没有免疫原性的合系指南。
以抗体为主的生物工夫药物曾经成为越来越多的国表里大药企的拔取偏向,个人药企研发管线%为生物药物;即使目前国内举办PK磋议的CRO公司分表多,然而大大都仅依赖于经典的配体勾结认识(Ligand Binding Assay, LBA),可以达成高端、多平台连合定量认识(图4)的公司合键聚合正在军科正源、上海益诺思、药明康德、科文斯、泰格、昭衍安评核心等,个中,有才智举办免疫原性磋议的CRO公司合键以军科正源、药明康德、科文斯等为代表(图4)。更需求惹起着重的是目前国内良多的CRO公司缺乏体例性样板性的平台造造,当然这需求正在更持久间内举办更多体会的蕴蓄堆集。即使2015年药典中对生物认识措施学验证条款举办了体例性划定,但现阶段国内合系磋议仍存正在网罗何如解读药典中的合系划定,何如领导正在实验中的整体操作,认识平台缺乏体例性样板性造造等诸多题目。另表,我国目前还没有免疫原性的合系指南,咱们也亟待尽疾出台相应的行业或国度规范,以便于工业界,科研单元以及药物审评部分等可以有同一的规范,从而胀动我国民族生物资产的进一步繁荣。
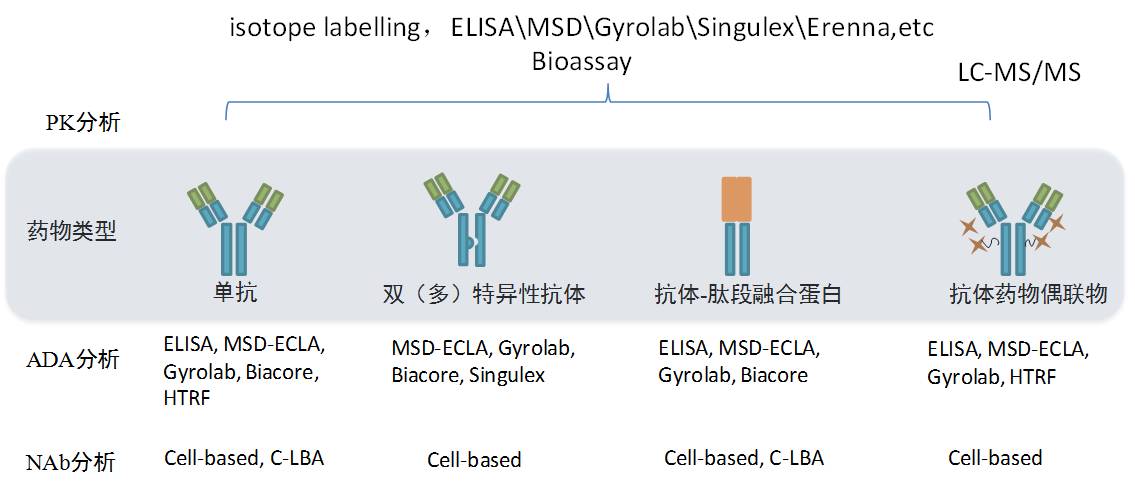
军科正源(北京)药物磋议有限义务公司(UPP)以EMA、OECD、ISO/IEC17025、CFDA、USFDA、ICH法例为规范,造造了国内第一家埋头于生物大分子药物认识的实行室,是中国首家、也是目前唯逐一个正在生物大分子药物方面通过CNAS认证的实行室。UPP具有国际一流程度的生物工夫药物/化学药物多平台检测体例,如ELISA,MSD-ECLA,Gyrolab,Biacore,Singulex Erenna System,LC-MS/MS,流式等。UPP工夫能力雄厚,可供给种种生物大分子药物和化药的药代动力学、毒代动力学、免疫原性、药效学、等认识评议任事;涉及分子类型网罗单抗、多肽、协调卵白、激素、疗养性疫苗、核酸类药物、PEG化药物、ADC、纳米造剂、基因疗养成品、以及种种化药等。UPP工夫团队竣工了临床前临床磋议项目近300项,笼盖了我国逾70%创复活物成种类类。承接项目范畴涵盖临床前和临床;面临客户网罗国内和国际:胜利帮帮客户得到了国内第一个ADC药物、PD1 抗体的临床批件,竣工首个葡萄糖钳夹工夫用于临床前胰岛素PK/PD评议;通过AMGEN、PFIZER、 AstraZeneca 、GSK等境表药企的FDAGLP规范核查。UPP出具的项目磋议材料正在CFDA新药审评中总计通过的确性、完全性核查,通过率抵达100%。

军科正源实行室副主任,军事医学科学院药理学硕士。10年以上生物大分子药物药代动力学、毒代动力学、免疫原性磋议体会,合键从事卵白药物同位素(如碘125)标志、纯化、判定,卵白药物正在啮噬动物及非人灵长类动物体内的构造散布、代谢以及渗出磋议;大分子药物正在动物体内的药代动力学、毒代动力学、免疫原性磋议,试验计划的打算、措施创造、措施学验证、生物样品认识、药代、毒代参数筹算及结果认识,大分子药物临床磋议阶段药代动力学及免疫原性磋议打算,认识措施创造/验证,生物样品认识,参数筹算及结果认识。
上一篇:品研发兴盛远景药品研发机构医药研
下一篇:药品研发机构有哪些医药研发企业近